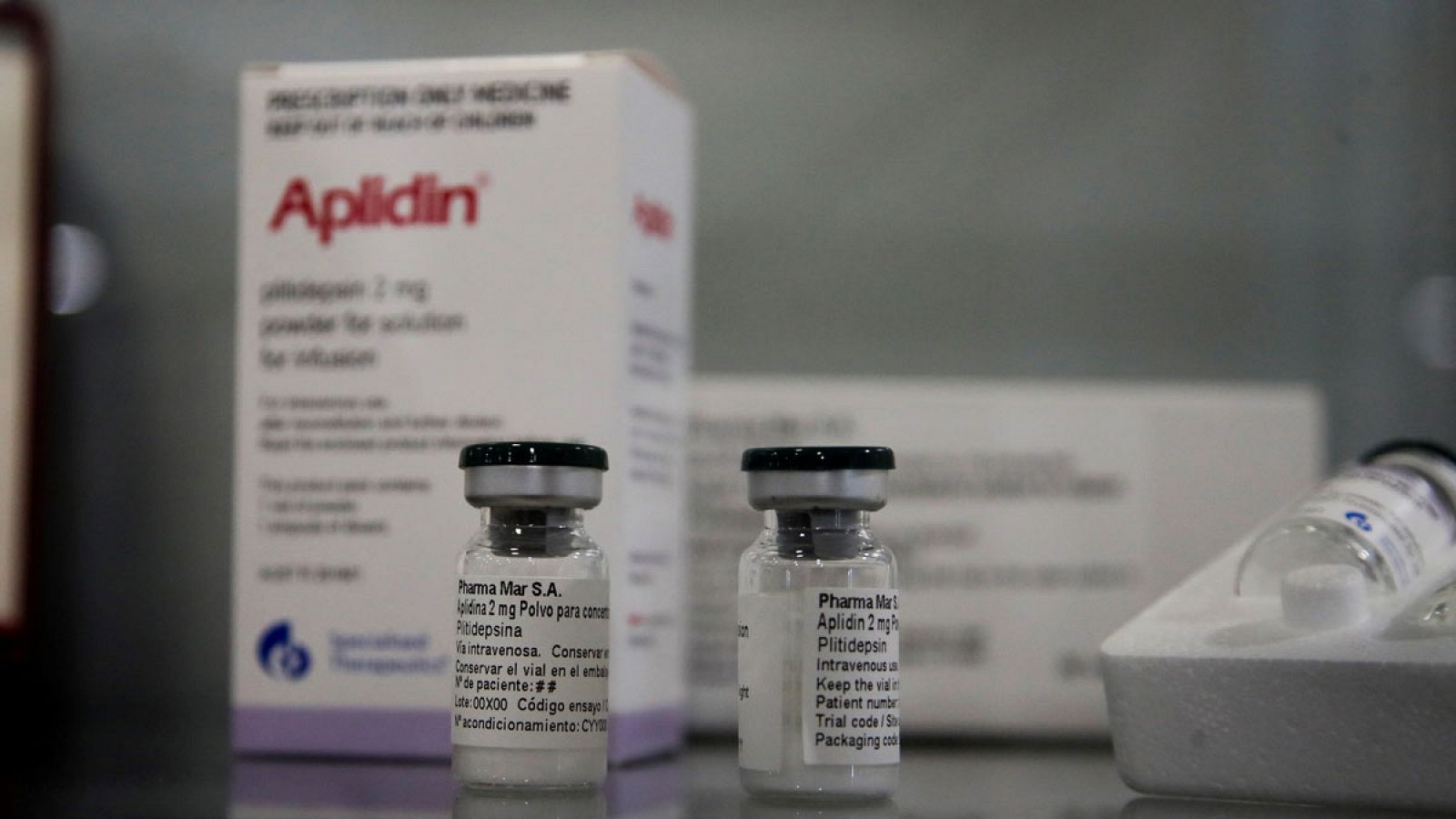
Aplidin, el antiviral de la farmacéutica española PharmaMar, reduce casi al 100% la carga del SARS-CoV-2
- Un estudio publicado en Science concluye que es el compuesto más potente contra el coronavirus que existe
- Coronavirus: última hora en directo | Mapa de España | Evolución de la curva | Hospitales y UCI
- Vacunas en España | Guía de restricciones | Mapa mundial
Aplidin, el fármaco antiviral de la empresa española PharmaMar basado en la plitidepsina y probado en laboratorios experimentales de Francia y Estados Unidos, ha demostrado una disminución del 99% de las cargas virales de SARS-CoV-2 en modelos animales.
Los experimentos tanto "in vitro como "in vivo" han certificado una eficacia antiviral y un perfil de toxicidad muy prometedores, resultados que han sido publicados en la revista Science. Los autores del estudio han concluido que la plitidepsina es "con diferencia" el compuesto más potente descubierto hasta ahora para el tratamiento de la COVID-19 y han planteado por ello que debería probarse en ensayos clínicos ampliados.
Aplidin es un medicamento que fue desarrollado inicialmente para tratar tumores, aunque debido a las características de su mecanismo de acción ha sido reposicionado para evaluar su efecto contra el coronavirus. La compañía farmacéutica española ya ha realizado estudios clínicos en fase 1 y 2 de este medicamento, con una pequeña muestra de pacientes, y quiere poner en marcha "lo antes posible" la tercera y última fase, previa a la comercialización, con una muestra mucho mayor que permita comparar los resultados del fármaco con los tratamientos actuales contra el coronavirus, principalmente corticoides.
El trabajo ha sido fruto de la colaboración entre la española PharmaMar y los laboratorios de los investigadores Kris White, Adolfo García-Sastre y Thomas Zwaka, en los Departamentos de Microbiología y de Biología Celular, Regenerativa y del Desarrollo, en la Icahn School of Medicine del Monte Sinai (Nueva York); de los científicos Kevan Shokat y Nevan Krogan, en el Instituto de Biociencias Cuantitativas de la Universidad de California San Francisco, y de Marco Vignuzzi, en el Instituto Pasteur de París.
Potencia antiviral y toxicidad limitada
Los autores han determinado que “la actividad antiviral de la plitidepsina contra el SARS-CoV-2 se produce mediante la inhibición de una conocida diana (la eEF1A)” y han asegurado que este fármaco ha demostrado "in vitro" una fuerte potencia antiviral, en comparación con otros antivirales contra el SARS-CoV-2, y además con una toxicidad limitada.
En dos modelos animales diferentes de infección por el coronavirus SARS-CoV-2 el ensayo demostró la reducción de la replicación viral, y se comprobó una disminución del 99% de las cargas virales en el pulmón de los animales tratados con plitidepsina.
La publicación concluye que este compuesto actúa bloqueando la citada proteína (a eEF1A), que está presente en las células humanas, y que es utilizada por el SARS-CoV-2 para reproducirse e infectar a otras células. “Creemos que nuestros datos y los resultados positivos iniciales del ensayo clínico de PharmaMar sugieren que plitidepsina debería considerarse seriamente para ampliar los ensayos clínicos para el tratamiento de COVID-19", han observado los investigadores.
El catedrático en el Departamento de Microbiología de la Escuela de Medicina Icahn del Monte Sinaí, Adolfo García-Sastre, ha informado de que de todos los inhibidores del SARS-CoV-2 que han clasificado en cultivo de tejidos y en modelos animales desde que iniciaron sus estudios con el SARS-CoV-2, plitidepsina ha sido el "más potente", lo que subraya su potencial como terapia para el tratamiento del COVID-19.
"Plitidepsina es un inhibidor extremadamente potente del SARS-CoV-2, cuya principal ventaja es que se dirige a una proteína de las células humanas y no a una proteína del virus. Esto significa que si plitidepsina tiene éxito en el tratamiento del COVID-19, el virus del SARS- CoV-2 no podrá hacerse resistente frente al tratamiento mediante mutaciones, lo que representa una gran preocupación con la actual propagación de las nuevas variantes del Reino Unido y Sudáfrica", ha apostillado el profesor adjunto del Departamento de Microbiología de la Escuela de Medicina Icahn del Monte Sinaí, Kris M. White.